
症例は臨床症例の一部を紹介するも ので、全ての症例が同様な結果を示すわ けではありません。
診断時の年齢:3歳
診断までにかかった時間:
診断につながった症状:心雑音
診断医:小児循環器科
ムコ多糖症VI型の患者さん(0~17歳)
内容1:
概要:
早い段階でムコ多糖症VI型と診断されたので、介入と管理を早くから進めることができました。このことが臨床転帰の向上につながっています。2
ムコ多糖症の古典的な症状(低身長、反復性中耳炎、骨格症状、リウマチ症状)に心臓障害が併発している場合は、遺伝疾患か代謝疾患の専門医へ直ちに照会してください。2
酵素補充療法(ERT)を開始
症例は臨床症例の一部を紹介するも ので、全ての症例が同様な結果を示すわ けではありません。
内容1:
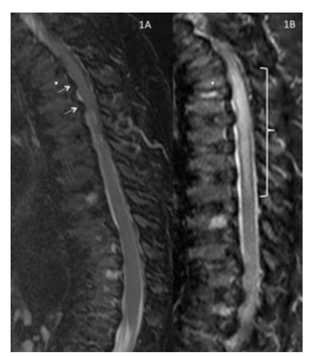
手術の7ヵ月前に撮影した胸椎・腰椎領域の画像(矢状断T2/短時間T1反転回復強調画像)
画像はDrummond社からの許可を得て複製しています(Can J Anesth, 2015)。
概要1:
この画像のケースでは、確認されていた脊柱管狭窄症の重症度とは釣り合わない術後脊髄損傷が生じています。ムコ多糖症IVA型(モルキオ症候群A型)患者さんにおいては、脊髄圧迫と脊髄損傷に対する脆弱性が極めて高いことが分かるケースです。
脊柱関節弛緩を伴う無症候性の脊柱管狭窄症は、圧迫リスクを高めます。麻酔科医は、この点を考慮しなければなりません。2
本ケースの経緯1
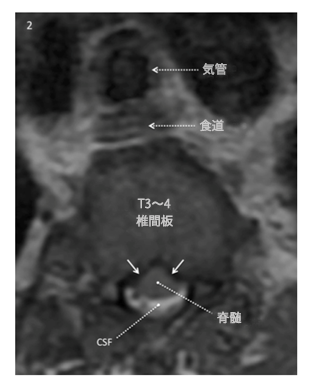
手術の7ヵ月前に撮影されたT3-4椎間板位の体軸断T2強調画像では、脊髄の前側ではなく後側の周辺に、脳脊髄液(CSF:白色箇所)が認められます。脊髄の前面は滑らかというよりも「突起状」になっており、脊髄前面に左右から圧力がかかっていることが分かります(白色矢印が指している箇所)。
画像はDrummond社からの許可を得て複製しています(Can J Anesth, 2015)。
症例は臨床症例の一部を紹介するも ので、全ての症例が同様な結果を示すわ けではありません。
Zakharchuk博士によって紹介されたケーススタディに基づいています。
内容1:
本ケースの経緯1
概要1
早期診断はERT開始(可能な場合)の鍵であり、患者さんの転帰を向上させるきっかけとなります。4-7,b 本ケースが示すように、ERTには、持久力や呼吸機能の測定値といった重要な臨床的パラメーターを改善する効果があり、患者さんの生活の質や歩行能力の維持、日常活動にとって決定的な要素となる可能性があります。8,9
症例は臨床症例の一部を紹介するも ので、全ての症例が同様な結果を示すわ けではありません。
診断時の年齢:12歳
診断までにかかった時間:11年
診断につながった症状:運動と言葉の遅れ
診断医:遺伝疾患の専門医
1歳のときに神経症状が現れ、その後発育遅延が急速に進行したことから、2人の姉妹はムコ多糖症IIIA型と診断されました1
内容1:
概要1:
本ケースが示しているとおり、ムコ多糖症IIIA型の患者さんにおいては、徴候と症状が、特に神経学的な状態の悪化と発育遅延の悪化を伴って急速に進行する可能性があります。ムコ多糖症を示す何らかの特徴がみられるお子さんが数人いらっしゃるご家族については、特に強い疑いを持ってください。1
継続的なモニタリングと評価も重要ですが、診断を早めるには、尿中GAGを使った代謝スクリーニングよりも、遺伝疾患や代謝疾患の専門医に直接照会することによって、早い段階から介入していくことが推奨されます。1
本ケースの経緯1
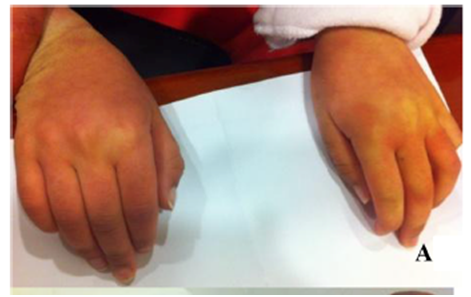
ムコ多糖症IIIA型の患者さんの場合、検査によって明らかな皮膚変色を確認することができます。1
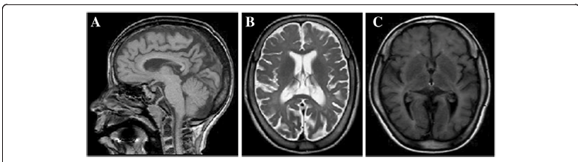
MRIでは、びまん性ミエリン形成不全、脳梁の菲薄化、中等度の大脳萎縮、長い時間をかけて徐々に現れた症状が確認されました。1
References: 1. Data on file. Biomarin Pharmaceutical. 2. Hendriksz CJ, Berger KI, Giugliani R, et al. International guidelines for the management and treatment of Morquio A syndrome. Am J Med Genet Part A. 2014;9999A:1-15. doi:10.1002/ajmg.a.36833. 3. Giugliani R, Lampe C, Guffon N, et al. Natural history and galsulfase treatment in mucopolysaccharidosis VI (MPS VI, Maroteaux-Lamy syndrome)–10-year follow-up of patients who previously participated in an MPS VI Survey Study. Am J Med Genet A. 2014;164A(8):1953-1964. doi:10.1002/ajmg.a.36584.
References: 1. Drummond JC, Krane EJ, Tomatsu S, Theroux MC, Lee RR. Paraplegia after epidural-general anesthesia in a Morquio patient with moderate thoracic spinal stenosis. Can J Anesth. 2015;62(1):45-49. doi:10.1007/s12630-014-0247-1. 2. Spinello CM, Novello LM, Pitino S, et al. Anesthetic management in mucopolysaccharidoses. ISRN Anesthesiol. 2013;2013:1-10. doi:10.1155/2013/791983.
References: 1. Data on file. Biomarin Pharaceutical. 2. Hendriksz CJ, Berger KI, Giugliani R, et al. International guidelines for the management and treatment of Morquio A syndrome. Am J Med Genet Part A. 2014;9999A:1-15. doi:10.1002/ajmg.a.36833. 3. Valayannopoulos V, Nicely H, Harmatz P, Turbeville S. Mucopolysaccharidosis VI. Orphanet J Rare Dis. 2010;5:5. doi:10.1186/1750-1172-5-5. 4. Clarke LA. Pathogenesis of skeletal and connective tissue involvement in the mucopolysaccharidoses: glycosaminoglycan storage is merely the instigator. Rheumatology (Oxford). 2011;50(suppl 5):v13-18. doi:10.1093/rheumatology/ker395. 5. Lehman TJA, Miller N, Norquist B, Underhill L, Keutzer J. Diagnosis of the mucopolysaccharidoses. Rheumatology. 2011;50(suppl 5):v41-v48. 6. Morishita K, Petty RE. Musculoskeletal manifestations of mucopolysaccharidoses. Rheumatology. 2011;50(suppl 5):v19-v25. doi:10.1093/rheumatology/ker397. 7. Muenzer J. Overview of the mucopolysaccharidoses. Rheumatology. 2011;50:v4-v12. doi:10.1093/rheumatology/ker394. 8. Hendriksz C. Improved diagnostic procedures in attenuated mucopolysaccharidosis. Br J Hosp Med. 2011;72(2):91-95. 9. Muenzer J. Early initiation of enzyme replacement therapy for the mucopolysaccharidoses. Mol Genet Metab. 2014;111(2):63-72. doi:10.1016/j.ymgme.2013.11.015.
Reference: 1. Sharkia R, Mahajnah M, Zalan A, Sourlis C, Bauer P, Schöls L. Sanfilippo type A: new clinical manifestations and neuro-imaging findings in patients from the same family in Israel: a case report. J Med Case Rep. 2014;8:78. doi:10.1186/1752-1947-8-78.